従来技術の内容と問題点
従来、脊椎動物においては転移活性を有するトランスポゾンが発見されておらず、トランスポゾンを用いた遺伝学的方法論は開発されてこなかった。
1990年代後半 従来脊椎動物で利用可能なトランスポゾンは存在しなかった。
⇩
1990年代後半〜2000年代前半 わが国発の技術Tol2トランスポゾン転移システムの開発
⇩
現在 脊椎動物研究で使われる三大トランスポゾン(❶Tol2 ❷Sleeping Beauty ➌Piggy Bac)
従来技術とTol2トランスポゾンの比較表
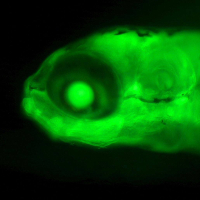
以下に、トランスジェニックゼブラフィッシュの作製、トランスジェニックマウスの作製、哺乳動物培養細胞への遺伝子導入について、従来法と本研究のトランスポゾンを用いた方法の比較を表す。
| 従来法 | Tol2トランスポゾンを用いた方法 | |
| トランスジェニックゼブラフィッシュの作製 | プラスミドDNAの受精卵への微量注入。 短所:効率が悪い。他コピー挿入されゲノム異常も伴う。発現のサイレンシングも起きうる。 |
トランスポゾン転移システムの受精卵への微量注入。 長所:10倍以上の効率上昇。単一コピー挿入で、ゲノム異常を伴わない。組み込まれた外来遺伝子は良く発現する。巨大DNA(100kb以上)の導入も可能。 |
| トランスジェニックマウスの作製 | プラスミドDNAの受精卵の核への微量注入。 短所:効率が悪い。他コピー挿入されゲノム異常も伴う。発現のサイレンシングも起きうる。 |
トランスポゾン転移システムの受精卵の核、細胞質への微量注入。 長所:10倍以上の効率上昇。単一コピー挿入で、ゲノム異常を伴わない。組み込まれた外来遺伝子は良く発現する。巨大DNA(100kb以上)の導入も可能。 |
| 哺乳動物培養細胞への遺伝子導入 | プラスミドDNAのエレクトロポレーション、トランスフェクション試薬による導入。 短所:プラスミドDNAは効率が悪い。他コピー挿入され、ゲノム異常も伴う。発現のサイレンシングも起きうる。レトロウイルスは操作が簡単でない。特殊な設備を要する。 |
トランスポゾン転移システムのエレクトロポレーション、トランスフェクション試薬による導入。 長所:10~100倍以上の効率上昇。単一コピー挿入で、ゲノム異常を伴わない。組み込まれた外来遺伝子は良く発現する。巨大DNA(100kb以上)の導入も可能。レトロウイルスに比較すると操作がはるかに簡単。 |
Tol2トランスポゾン技術について関連記事
ご確認いただいて、お問合せくださいませ。